El cultivo in vitro (término que literalmente significa en vidrio), incluye muchas técnicas destinadas a introducir, multiplicar y regenerar, entre otros recursos, material vegetal o animal en condiciones controladas y asépticas.
à El cultivo in vitro, constituye un paso fundamental en la obtención y regeneración de plantas genéticamente modificadas, o transgénicas, mediante técnicas de ingeniería genética. Es decir que existe una estrecha relación entre el cultivo de tejidos vegetales y la biotecnología moderna. Normalmente se utilizan cultivos de tejidos, seguido de la regeneración de la planta completa, y la subsiguiente expresión de los genes introducidos, o transgenes.
Cultivo in Vitro de material vegetal “Cultivo de tejidos vegetales” es una descripción genérica que involucra diferentes técnicas de cultivo de material vegetal diverso, incluyendo las de protoplastos (células desprovistas de su pared celular), células, tejidos, órganos y plantas completas. Mediante éstas y otras técnicas de cultivo, es posible obtener plantas libres de microbios en un medio nutritivo aséptico (estéril) en condiciones ambientales controladas. Las primeras experiencias relacionadas al cultivo de tejidos vegetales se remontan a 1902, pero recién en 1922 se logró el primer experimento exitoso: germinación in vitro de semillas de orquídeas. Luego de la germinación, las plántulas obtenidas se transfirieron a un medio de cultivo en condiciones asépticas, y así se mantuvieron protegidas del ataque de patógenos (hongos, virus y bacterias).
Esta técnica tiene numerosas aplicaciones.
•
|
Propagación masiva de plantas, especialmente beneficiosa para especies de difícil
|
•
|
propagación por otros métodos, o en vías de extinción
|
•
|
Obtención de plantas libres de virus
|
•
|
Producción de semillas sintéticas
|
•
|
Conservación de germoplasma: material de un conjunto de individuos que representa la variabilidad genética de una población vegeta
|
Respecto del proceso de transformación vegetal, existen distintas técnicas para la transferencia de genes a las células vegetales, siendo las principales la interacción con bacterias del género Agrobacterium y el método de Biobalística. Una vez realizada la transformación genética por alguno de estos dos métodos, el paso siguiente es el cultivo in vitro, con el fin de regenerar plántulas a partir del explanto inicial transformado, proceso que se sustenta en el principio de “totipotencialidad celular”. De aquí la importancia del cultivo in vitro como paso fundamental para la obtención y regeneración de plantas genéticamente modificadas.
à La Micropropagación es el conjunto de técnicas y métodos de cultivo de tejidos utilizados para multiplicar plantas asexualmente en forma rápida, eficiente y en grandes cantidades.
La micropropagación se utiliza para multiplicar o propagar plantas nuevas, tales como aquellas creadas por ingeniería genética, mutagénesis o mejoramiento genético. Se utiliza también la micropropagación para obtener plantas libres de enfermedades (tales como virosis) u obtener grandes cantidades de plantas que no se propagan eficientemente. La micropropagación constituye la principal aplicación comercial del cultivo de tejidos vegetales.
Existen dos posibles vías morfogenéticas implicadas en la diferenciación.
à La organogénesis es de origen pluricelular. Un grupo de células del explante inicial se desdiferencía inicialmente para luego rediferenciarse dando lugar a un órgano vegetal.
à La embriogénesis se presupone de origen unicelular. Una célula del explante se aísla y constituye el punto de partida para la obtención de un embrión somático. Se diferencian embriones o estructuras bipolares que completan cada una de las etapas implicadas en la ontogenia de un embrión cigótico. El resultado es una planta completa. Etapas implicadas en el protocolo de micropropagación de una especie vegetal.
La tecnología para la obtención de plantas libres de patógenos es de gran utilidad para obtener altos rendimientos en cultivos de propagación vegetativa. El proceso pasa por dos etapas bien definidas, la primera es la etapa de laboratorio y la segunda es la etapa de invernadero. Ambas están estrechamente relacionadas, ya que para poder propagar plantas en invernaderos se debe contar con material procedente de cultivo de tejidos de laboratorio. La propagación en invernaderos se caracteriza por que la propagación de las plantas que se instalan se realiza en un ambiente protegido del ingreso de insectos vectores trasmisores de virus, además de otras plagas. De igual modo el uso de sustrato desinfectado permite una propagación libre de patógenos y el uso de plántulas libres de virus procedentes de propagación ‘in vitro’.
El cultivo de anteras es una técnica para la producción de haploides y/o plantas diploides las cuales son un gran potencial para los mejoradores de plantas. La haploidía puede intervenir en el mejoramiento de las plantas autógenas de dos modos diferentes. De una parte, ella facilita la identificación y selección de mutantes recesivos a nivel de plantas y de células. De otra parte, la inducción de haploides en los híbridos, seguido de un doblamiento cromosómico permite la obtención de líneas perfectamente homocigóticas evitando una larga serie de autofecundaciones.
El cultivo de anteras ha demostrado ser una técnica útil para acelerar la introgresión de características deseables en poblaciones de mejoramiento. Pero el uso de la técnica del cultivo de anteras se ha visto limitada por la baja frecuencia de producción de callos y regeneración de plantas verdes en genotipos. Varios investigadores han notado que la inducción de callos y la regeneración de plantas verdes están influenciados por el genotipo utilizado, el estado de desarrollo de la microspora, las condiciones de desarrollo de los padres donantes (fotoperíodo e intensidad de la luz), tratamiento físico de las anteras antes de su inoculación, medio definido, etc.
La variación somaclonal puede usarse, con muchas frecuencias, para recuperar la variación genética natural de una variedad. La variación somaclonal es superior también al mejoramiento por mutaciones inducidas puesto que en las plantas regeneradas que derivan de células individuales, la ocurrencia de mosaicos es mínima. En la mayor parte de los casos, por tanto, los somaclones pueden estabilizarse en una generación; las mutaciones, en cambio requieren varias generaciones y retrocruces. La variación somaclonal puede causar una variación temporal (epigenetica) o una variación genética. Por definición, los cambios epigeneticos no se transmiten meioticamente, razón por la cual no son útiles en el fitomejoramiento. Una variación fenotípica tiene valor en el fitomejoramiento si proviene de una verdadera modificación del material genético.
Los protoplastos constituyen un explanto ideal para diferentes aplicaciones biotecnológicas. La ausencia de pared celular rígida y la completa exposición de la membrana plasmática hacen de los protoplastos un sistema útil para el estudio de los fenómenos de transporte a través de esta última. Numerosas investigaciones acerca del proceso de infección y replicación de virus fitopatógenos se han valido de los protoplastos como herramienta de indagación. También han sido utilizados para la elucidación de la especificidad y modo de acción de patógenos fúngicos y bacterianos. Los protoplastos aislados son capaces de incorporar organelas exógenas, tales como núcleos y cloroplastos, así como también ADN, proteínas, y otras macromoléculas, lo que posibilitó el desarrollo de ensayos de transformación genética y de fusión. Estos explantes pueden ser empleados con éxito en ensayos de mutagénesis y la regeneración posterior de plantas transgénicas.
Las aplicaciones agronómicas son;
à Mejora genética.
à Propagación masiva.
à Plantas libres de patógenos.
à Conservación del germoplasma.
à Metabolitos secundarios.
à Investigación.
La conservación in vitro tiene que considerarse como parte de la estrategia general de conservación de una especie vegetal, es más bien un auxiliar valioso y un suplemento de la conservación de los recursos genéticos. Solo ocasionalmente, el almacenamiento in vitro sería la única estrategia para conservar una especie dada. Para algunos frutales tropicales como el cacao (Theobrama), la estrategia principal de conservación estaría probablemente en los bancos genéticos in vitro que utilizan las técnicas in vitro para evaluar la variabilidad genética de las especies, y para la colección e intercambio de esta. Los cultivos de raíces y tubérculos, como papa, yuca y batata (Ipomoea), se almacenarían como semilla durante cortos periodos, de modo que, para ellos, los métodos in vitro serian complementarios para la conservación de genotipos específicos (cultivares, híbridos, clones elite) y para el traslado internacional de clones. Para otros cultivos de tubérculos y raíces tropicales y para especies de frutales como Musa spp., que rara vez producen semilla y son prácticamente estériles, el almacenamiento in vitro y los bancos genéticos es situ en el campo estarían probablemente a la par.
Los métodos de conservación
à Crecimiento normal
Transferencia seriada
à Metabolismo limitado
Baja concentración nutricional, gelificante, etc.
à Metabolismo detenido
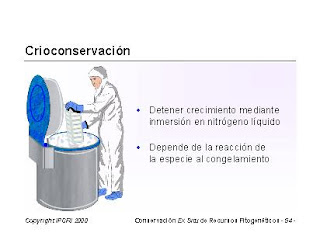
Crioconservación
Esta última, implica la conservación de los explantes a temperaturas ultrabajas del nitrógeno líquido (-196ºC) y se denomina crioconservación. La crioconservación es una valiosa herramienta para conservar a largo plazo (años) nuestros recursos Fitogenéticos, ofreciendo la máxima estabilidad de los caracteres genotípicos del germoplasma conservado, así como mínimos requerimientos de espacio y mantenimiento. Actualmente se dispone de varias técnicas para la crioconservación de germoplasma vegetal, entre las cuales se encuentra la encapsulación-deshidratación. El uso de la crioconservación para el almacenamiento de germoplasma ofrecen varias ventajas en relación con las técnicas tradicionales, pues permiten la conservación a largo plazo (años), con bajos costos de mantenimiento, fácil manipulación de las muestras y no dependen del suministro eléctrico.